Calor intercambiado a partir de energía interna y trabajo
Enunciado
¿Qué calor se intercambia en un proceso cuando se realiza un trabajo de 850 J, sabiendo que la diferencia de energía interna entre sus estados inicial y final es de 3 kJ? Suponiendo que el trabajo lo realiza un gas a una presión de 2 atm, ¿qué variación de volumen tiene lugar en el proceso?
Solución
Datos
- Variación de energía interna ∆U = 3kJ = 3·103 J
- Trabajo W = 850 J
- Presión p = 2 atm = 2·101325 = 202650 Pa
Consideraciones previas
-
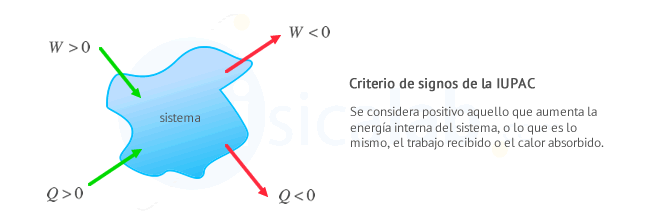
Usaremos el criterio de signos propio de la IUPAC según el cual el trabajo es positivo cuando aumenta la energía interna del sistema
Resolución
La primera ley de la termodinámica establece la relación entre trabajo termodinámico, calor intercambiado y variación de energía interna. Así, nos queda:
En cuanto a la variación de volumen experimentada por el gas, lo calculamos aplicando la expresión del trabajo termodinámico:
Es decir, el gas reduce su volumen.
Fórmulas
Estas son las principales fórmulas que debes conocer para resolver este ejercicio. Si no tienes claro su significado, te recomendamos que consultes la teoría de los apartados relacionados. Además, en ellos encontrarás, bajo la pestaña Fórmulas, los códigos que te permitirán integrar estas fórmulas en programas externos como por ejemplo Word o Mathematica.
